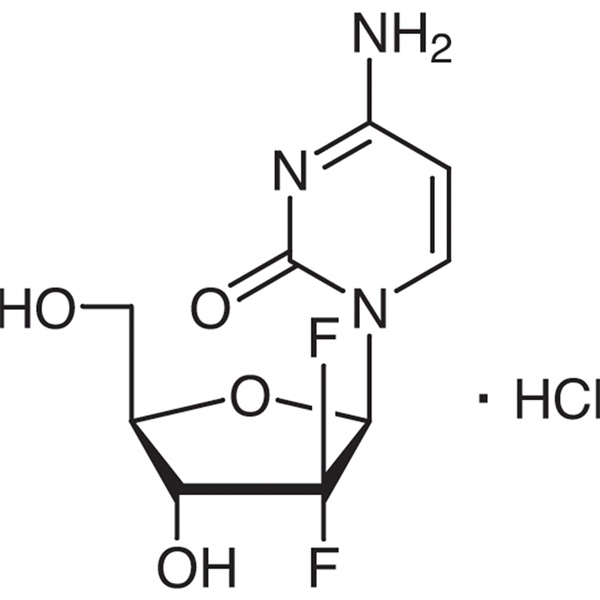
젬시타빈 염산염 CAS 122111-03-9 API USP35 표준
Ruifu Chemical은 고품질의 상업 생산을 갖춘 Gemcitabine Hydroclide(CAS: 122111-03-9)의 선도적인 제조업체입니다. Ruifu Chemical은 전세계 배송, 경쟁력 있는 가격, 우수한 서비스, 소량 및 대량 수량을 제공할 수 있습니다. 젬시타빈 염산염 구매, 문의처: alvin@ruifuchem.com
| 화학명 | 젬시타빈 염산염 |
| 동의어 | 젬시타빈 HCl; 2'-데옥시-2',2'-디플루오로시티딘 염산염; dFdC; dFdCyd; 젬자르; LY188011 염산염; 젬시테라; 젬사르 |
| CAS 번호 | 122111-03-9 |
| 관련 CAS | 95058-81-4 - 무료 베이스 |
| 재고현황 | 재고 있음, 생산 능력 5톤 |
| 분자식 | C9H12ClF2N3O4 |
| 분자량 | 299.66 |
| 녹는점 | >250℃ |
| 배송조건 | 주변 온도에서 |
| COA 및 MSDS | 가능 |
| 원산지 | 중국 상하이 |
| 브랜드 | 루이푸 화학 |
| 품목 | 사양 | 결과 |
| 외관 | 백색 결정성 분말, 무취 | 준수 |
| 용해도 | 물에 용해되고, 메탄올에 약간 용해되며, 아세톤에 거의 녹지 않음 | 준수 |
| 식별IR | IR 스펙트럼은 다음과 일치해야 합니다. 참조 표준의 것 | 준수 |
| 식별 염화물 | 긍정적입니다. 염화물 테스트 요구 사항을 충족합니다. | 준수 |
| 솔루션의 모습 | 솔루션 S는 명확하고 더 강하지 않습니다. 기준액 BY7보다 착색됨 | 준수 |
| pH | 2.0~3.0 | 2.6 |
| 특정 회전 [α]20/D | +43.0° ~ +50.0° | +47.5° |
| 중금속(Pb) | 10ppm 이하 | <10ppm |
| 건조 감량 | 1.00% 이하 | 0.3% |
| 점화 잔류물 | 0.10% 이하 | 0.03% |
| 관련 물질 | ||
| 시토신 | 0.10% 이하 | 0.01% |
| α-이성체 | 0.10% 이하 | 0.01% |
| 기타 불순물 | 0.10% 이하 | 0.04% |
| 총 불순물 | 0.20% 이하 | 0.1% |
| 잔류용매 | ||
| 메탄올 | 0.30% 이하 | 감지되지 않음 |
| 톨루엔 | 0.01% 이하 | 감지되지 않음 |
| 디클로로메탄 | 0.01% 이하 | 감지되지 않음 |
| 아세톤 | 0.50% 이하 | 0.1% |
| 분석 | 97.5%~101.5% (건조원료로 계산) | 99.9% |
| 결론 | USP35 표준을 준수합니다. | |
패키지: 병, 알루미늄 호일 백, 25kg/Cardboard Drum 또는 고객 요구 사항에 따라.
보관 조건: 용기를 단단히 밀봉하여 서늘하고 건조하며 통풍이 잘되는 창고에 보관하고, 배합 금지 물질이 없는 곳에 보관하십시오. 직사광선, 습기 및 과도한 열에 노출되지 않도록 하십시오.
배송: FedEx / DHL Express를 통해 항공으로 전 세계로 배송됩니다. 빠르고 안정적인 배송을 제공합니다.

위험 코드 R21 - 피부와 접촉하면 유해함
R36/38 - 눈과 피부에 자극적입니다.
R46 - 유전적 유전적 손상을 일으킬 수 있음
R62 - 생식력 장애의 위험 가능성
R63 - 태아에게 해를 끼칠 위험이 있음
안전 설명 S25 - 눈과의 접촉을 피하십시오.
S26 - 눈에 들어간 경우 즉시 다량의 물로 씻어내고 의사의 진료를 받으십시오.
S36/37 - 적절한 보호복과 장갑을 착용하십시오.
S53 - 노출을 피하세요 - 사용하기 전에 특별한 지침을 얻으십시오.
WGK 독일 3
RTECS HA3840000
HS 코드 2942000000
젬시타빈 염산염(CAS: 122111-03-9)은 항대사 및 항종양성인 합성 신규 디플루오로 뉴클레오시드 약물입니다. Eli Lilly and Company에 의해 연구 개발되었으며 1995년 남아프리카, 스웨덴, 네덜란드, 호주 및 기타 국가에 등재되도록 승인되었습니다. 미국 식품의약국(FDA)은 이를 비소세포폐암 및 췌장암의 임상 치료를 위한 1차 치료법으로 승인했습니다.
최근에는 비소세포폐암(NSCLC) 치료에 젬시타빈(Gemcitabine), 파클리탁셀(Paclitaxel), 도세탁셀(Docetaxel), 비노레빈(Vinorebine) 등의 신약이 효과적인 약물이 되고 있다. 이들 약물은 기존 화학요법 약물에 비해 치료 효과는 높고 독성은 낮다는 장점이 있다. 젬시타빈 염산염은 차세대 항대사 약물이자 세포 주기를 위한 특수 의약품의 일종으로, 세포의 DNA 합성 단계, 즉 세포의 S 단계에서 중요한 역할을 합니다. 특정 조건 하에서 이 약은 세포의 G1기에서 S기로의 진행을 예방할 수 있으며, 비소세포폐암(NSCLC)에 대한 강력한 항암 활성을 나타냅니다. 외국 연구에 따르면 젬시타빈 염산염 단독으로 NSCLC를 단독으로 치료할 때의 효율성은 약 18%~35%인 반면, 시스플라틴과 병용 치료할 경우 NSCLC의 효율성은 41.7%인 것으로 나타났습니다. 진행성 NSCLC에서 카보플라틴의 유효 비율은 16%로 시스플라틴과 유사하지만 독성이 낮으며, 특히 위장 반응, 골수 억제, 신장 및 신경 말단의 독성 반응에 효과적입니다. 카보플라틴과 결합하면 둘 다 상호 조정 및 부가 효과가 있어 더 높은 치료 효과를 얻을 수 있습니다.
젬시타빈 염산염
C9H11F2N3O4·HCl 299.66
시티딘, 2'-데옥시-2',2'-디플루로-, 모노염산염.
2'-데옥시-2',2'-디플루오로시티딘 모노염산염(β-이성질체) [122111-03-9].
» 젬시타빈 염산염은 현 상태 기준으로 계산하여 C9H11F2N3O4·HCl을 97.5% 이상 101.5% 이하로 함유합니다.
[주의사항-젬시타빈염산염은 강력한 세포독성제입니다. 입자를 흡입하고 피부가 노출되지 않도록 세심한 주의를 기울여야 합니다.]
포장 및 보관-단단한 용기에 보관하세요.
라벨링-주사 가능한 제형을 제조하는 데 사용하도록 의도된 경우, 라벨에는 멸균되었거나 주사용 제형을 제조하는 동안 추가 처리를 거쳐야 한다고 명시되어 있습니다.
USP 참조 표준<11>-
USP 시토신 RS
USP 내독소 RS
USP 젬시타빈 염산염 RS
신분증-
A: 적외선 흡수<197K>.
B: 염화물<191> 시험 요건을 충족합니다.
특정 회전 <781S>: 20에서 +43과 +50 사이.
시험 용액: mL당 10mg.
pH<791>: 2.0~3.0, mL당 10mg을 함유한 용액.
강열잔류물<281>: 0.1% 이하.
중금속, 방법 I<231>: 0.001%.
크로마토그래피 순도-
솔루션 A- 분석의 이동상 지시에 따라 진행합니다.
용액 B-여과 및 탈기된 메탄올을 준비합니다.
이동상-크로마토그래피 시스템의 지시에 따라 용액 A와 용액 B의 다양한 혼합물을 사용합니다. 필요한 경우 조정합니다(크로마토그래피 621의 시스템 적합성 참조).
시스템 적합성 솔루션-분석 지침에 따라 진행합니다.
표준액-정량의 USP 젬시타빈염산염표준품 및 USP 시토신표준품을 정확하게 달아 물에 녹이고 필요하면 단계적으로 정량적으로 희석하여 각각 약 2 µg/mL의 농도를 갖는 용액을 만든다.
검액-이 약 약 50 mg을 정확하게 달아 25 mL 용량플라스크에 취하고 물을 넣어 녹여 표선까지 희석하여 혼합한다.
크로마토그래피 시스템(크로마토그래피 621 참조)-분석 지침에 따라 진행합니다. 크로마토그래프는 다음과 같이 프로그래밍됩니다.
시간(분) 용액 A(%) 용액 B(%) 용출
0–8 97 3 등용매
8–13 97®50 3®50 선형 구배
13–20 50 50 등용매
20–25 50®97 50®3 재-평형
시스템 적합성 용액을 크로마토그래피하고 절차에 따라 피크 반응을 기록합니다. 상대 유지 시간은 젬시타빈 -아노머의 경우 약 0.5이고 젬시타빈의 경우 1.0입니다. 젬시타빈 -아노머와 젬시타빈 사이의 분리도 R은 8.0 이상이며; 젬시타빈의 테일링 인자는 1.5를 넘지 않습니다. 표준 용액을 크로마토그래피하고 절차에 따라 피크 반응을 기록합니다. 상대 체류 시간은 시토신의 경우 약 0.1이고 젬시타빈의 경우 1.0입니다. 반복 주입의 상대 표준 편차는 2.0%를 넘지 않습니다.
조작-표준액과 검액을 각각 크로마토그래프에 약 20 μL씩 주입하고 크로마토그램을 기록하여 모든 피크반응을 측정한다. 다음 공식에 따라 Gemcitabine 부분의 시토신 비율을 계산합니다.
2.5(CC/W)(rt/rs)
Cc는 표준용액 내 USP 시토신표준품의 농도(μg/mL)이다. W는 복용한 젬시타빈의 중량(mg)입니다. rt는 검액의 시토신에 대한 피크 반응이다. rs는 표준 용액의 시토신에 대한 반응입니다. 시토신이 0.1% 이하로 발견됩니다. 다음 공식에 따라 젬시타빈 부분에서 시토신을 제외한 각 불순물의 백분율을 계산합니다.
2.5(Cs/W)(ri/rs)
Cs는 표준액 중 USP 젬시타빈 염산염 표준품의 농도(mL당 µg)입니다. W는 복용한 젬시타빈의 중량(mg)입니다. ri는 시험 용액의 각 불순물에 대한 최고 반응이다. rs는 표준 용액의 젬시타빈으로 인한 반응입니다. 0.1% 이하의 젬시타빈 -아노머 또는 기타 개별 불순물이 발견됩니다. 모든 불순물의 합은 0.2%를 넘지 않아야 합니다. 모든 불순물의 합계에서 정량 한계(0.02%) 미만인 피크를 제외합니다.
기타 요구 사항-라벨에 젬시타빈 염산염이 멸균되어 있다고 명시되어 있는 경우 주사용 젬시타빈에 따른 세균 내독소 및 무균 요구 사항을 충족합니다. 주사용 제형을 준비하는 동안 젬시타빈 염산염이 추가 가공을 거쳐야 한다고 라벨에 명시되어 있는 경우 이는 주사용 젬시타빈에 따른 세균 내독소 요건을 충족합니다.
분석-
이동상-물 1000mL에 일염기성 인산나트륨 13.8g과 인산 2.5mL를 함유하는 여과 및 탈기 용액을 준비합니다. [참고-이 용액의 pH는 2.4~2.6입니다. ]
시스템 적합성 용액-이 약 10mg을 작은 바이알에 넣고 메탄올 1mL당 수산화칼륨 168mg을 함유한 용액 4mL를 첨가한 후 단단히 마개하고 초음파 처리합니다. 55℃에서 6~16시간 동안 가열하고 식힌 다음 내용물을 1%(v/v) 인산으로 연속 세척하면서 100mL 용량 플라스크에 옮깁니다. 1% 인산을 넣어 부피만큼 희석하고 혼합한다. [참고-이 용액에는 젬시타빈 α-아노머가 mL당 약 0.02mg 함유되어 있습니다.]
표준품-이 약 일정량을 정확하게 달아 물에 녹이고 필요하면 물로 단계적으로 희석하여 약 0.1mg/mL의 용액을 얻는다.
정량조제-이 약 약 20 mg을 정확하게 달아 200 mL 용량플라스크에 취하고 물을 넣어 녹여 표선까지 희석하여 혼합한다.
크로마토그래피 시스템(크로마토그래피<621> 참조)-액체 크로마토그래피에는 275-nm 검출기와 5-μm 패킹 L7을 포함하는 4.6-mm × 25-cm 컬럼이 장착되어 있습니다. 유속은 분당 약 1.2mL입니다. 시스템 적합성 용액을 크로마토그래피하고 절차에 따라 지시된 대로 피크 반응을 기록합니다. 젬시타빈 -아노머와 젬시타빈 사이의 분해능 R은 8.0 이상입니다. 젬시타빈으로부터 결정된 테일링 인자는 1.5 이하이다. 표준 준비를 크로마토그래피하고 절차에 따라 지시된 대로 피크 반응을 기록합니다. 반복 주입의 상대 표준 편차는 1.0%를 넘지 않습니다.
절차-표준액과 분석액을 같은 부피(약 20μL)씩 크로마토그래피에 별도로 주입하고 크로마토그램을 기록하고 주요 피크에 대한 반응을 측정합니다. 다음 공식에 따라 젬시타빈 염산염 부분에 포함된 C9H11F2N3O4·HCl의 양을 mg 단위로 계산합니다.
200C(rU/rS)
C는 표준액에 포함된 USP 젬시타빈 염산염 표준품의 농도(mg/mL)입니다. rU와 rS는 각각 분석 준비와 표준 준비에서 얻은 피크 반응입니다.