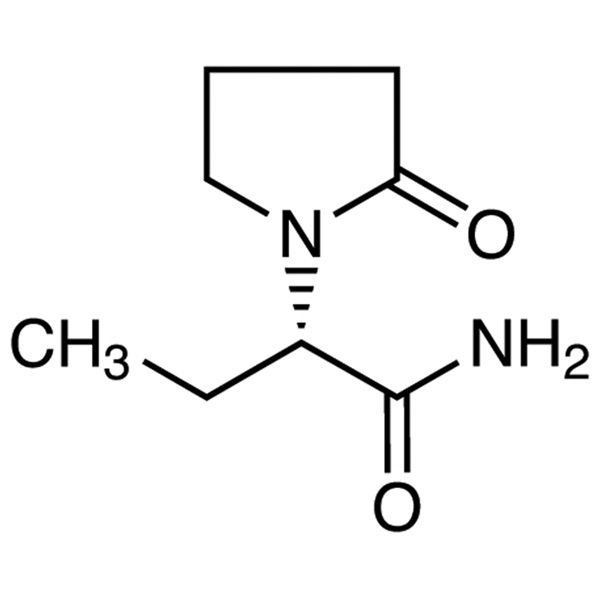
Levetiracetam LEV CAS 102767-28-2 분석실험 98.0%~102.0% USP EP 기준
Shanghai Ruifu Chemical Co., Ltd.는 고품질과 안정적인 품질, API, USP/EP 표준, 3세대 항간질제를 갖춘 Levetiracetam(CAS: 102767-28-2)의 선두 제조업체입니다. Ruifu Chemical은 전세계 배송, 경쟁력 있는 가격, 우수한 서비스, 소량 및 대량 수량을 제공할 수 있습니다. 레베티라세탐 구매, 문의처: alvin@ruifuchem.com
| 화학명 | 레베티라세탐 |
| 동의어 | 레프; (S)-2-(2-옥소-1-피롤리디닐)부티르아미드; UCB-L059; (S)-알파-에틸-2-옥소-1-피롤리딘아세트아미드; (2S)-2-(2-옥소피롤리딘-1-일)부탄아미드 |
| CAS 번호 | 102767-28-2 |
| 재고현황 | 재고 있음, 연간 생산 능력 500톤 |
| 분자식 | C8H14N2O2 |
| 분자량 | 170.21 |
| 녹는점 | 116.0~119.0℃ |
| 밀도 | 1.168g/cm3 |
| 용해도 | 아세톤에 용해됨 |
| COA 및 MSDS | 가능 |
| 제품의 원산지 | 중국 상하이 |
| 제품 카테고리 | 항간질제; API(활성 의약품 성분) |
| 브랜드 | 루이푸 화학 |
| 품목 | 사양 |
| 외관 | 흰색 또는 거의 흰색에 가까운 결정 분말 |
| 신분증 | IR |
| 솔루션의 모습 | BY6보다 선명하고 과하지 않은 컬러감 |
| 레베티라세탐 R-에난티오머의 한계 | 0.80% 이하 |
| 물 (by K.F) | 0.50% 이하 |
| 점화 잔류물 | 0.10% 이하 |
| 중금속 | 0.001% 이하 |
| 관련 물질 | |
| 피리딘-2-ol | 0.025% 이하 |
| 레베티라세탐산 | 0.30% 이하 |
| 레베티라세탐 관련 화합물 A | 0.05% 이하 |
| 레베티라세탐 관련 화합물 B | 0.10% 이하 |
| 모든 개별 불특정 불순물 | 0.05% 이하 |
| 총 불특정 불순물 | 0.10% 이하 |
| 총 불순물 | 0.40% 이하 |
| 잔류용매 | 사양을 충족 |
| 분석 / 분석 방법 | 98.0%~102.0% (무수물, 무용매 기준으로 계산) |
| 테스트 표준 | USP 표준; EP 표준 |
| 신청 | API; 3세대-세대 항간질제 |
패키지: 병, 알루미늄 호일 백, 25kg/Cardboard Drum 또는 고객 요구 사항에 따라.
보관상태: 용기를 단단히 밀봉한 후 서늘하고 건조하며 통풍이 잘되는 창고에 보관하십시오. 햇빛을 피하십시오. 화재 및 열원을 피하십시오. 습기를 피하십시오.
배송: FedEx/DHL Express를 통해 항공으로 전 세계로 배송됩니다. 빠르고 안정적인 배송을 제공합니다.
레베티라세탐
C8H14N2O2 170.21
1-피롤리딘아세트아미드, -에틸-2-옥소-, (S)-;
()-(S)--에틸-2-옥소-1-피롤리딘아세트아미드 [102767-28-2].
정의
레베티라세탐은 무수물과 용매를 기준으로 계산하여 NLT 98.0%와 NMT 102.0%의 C8H14N2O2를 함유하고 있습니다.
식별
• A. 적외선 흡수 <197K>
• B. 검액에서 나온 레비티라세탐 주요 피크의 머무름 시간은 레베티라세탐 R-거울상 이성질체 한계 시험에서 얻은 시스템 적합성 용액의 레비티라세탐 거울상 이성질체의 머무름 시간과 일치합니다.
분석
• 절차
완충액: 물에 용해된 일염기성 인산칼륨 2.7g/L. 2% 수성 수산화칼륨(w/v)을 사용하여 pH 5.5로 조정합니다.
솔루션 A: 아세토니트릴 및 완충액(1:19)
용액 B: 아세토니트릴
이동상: 아래 기울기 표를 참조하세요.
시간(분) 용액 A(%) 용액 B(%)
0 100 0
3 100 0
20 71 29
시스템 적합성 용액: 용액 A에 USP 레베티라세탐 RS 0.2 mg/mL 및 USP 레베티라세탐 관련 화합물 A RS 0.08 mg/mL. 먼저 적합한 용량 플라스크에 필요한 양의 USP 레베티라세탐 RS를 용해시켜 준비합니다. 플라스크 부피의 10%에 해당하는 0.1N 수산화칼륨을 첨가합니다. 혼합물을 실온에서 약 15분간 반응시킨 후, 플라스크 부피의 10%에 맞춰 0.1N 염산을 첨가하여 중화시킨다. 필요한 양의 USP 레베티라세탐 관련 화합물 A RS를 첨가하고 초음파 처리하여 용해시킨 다음 용액 A로 부피를 희석하고 혼합합니다.
표준 용액: 용액 A에 들어 있는 USP 레베티라세탐 RS 0.1mg/mL
샘플 용액: 용액 A 중 레베티라세탐 0.1 mg/mL
크로마토그래피 시스템
(크로마토그래피<621>, 시스템 적합성 참조)
모드: LC
검출기: UV 205nm
컬럼: 4.6-mm × 15-cm; 포장 L1
유속: 0.9mL/분
주입 크기: 10 µL
시스템 적합성
샘플: 시스템 적합성 솔루션
[참고-상대 체류 시간은 불순물 표 1에 나와 있습니다.]
적합성 요구 사항
상대 표준편차: NMT 1.0%
[참고-시스템 적합성 기준을 충족할 수 없는 경우 시스템 안정화를 위해 컬럼 온도를 20°C로 유지하는 것이 좋습니다.]
분석
시료: 표준용액 및 시료용액
레베티라세탐을 복용한 부분에서 C8H14N2O2의 비율을 계산합니다.
결과 = [(rU/rS) × (CS/CU) × 100] F
rU = 검체 용액의 레비티라세탐 피크 반응
rS = 표준 용액의 레비티라세탐 피크 반응
CS = 표준 용액 내 USP 레베티라세탐 RS의 농도(mg/mL)
CU = 검체 용액 내 레베티라세탐 농도(mg/mL)
F = 레베티라세탐 R-거울상 이성질체 한계 시험에서 얻은 레비티라세탐 R-거울상 이성질체의 백분율
허용 기준: 무수 및 용제 기준 98.0%-102.0%
불순물
무기 불순물
• 점화 잔류물<281>: NMT 0.1%
• 중금속, 방법 II<231>: 20ppm
유기 불순물
• 절차 1: 레베티라세탐 관련 화합물 B의 한도
[참고-레베티라세탐 관련 화합물 B가 알려진 공정 불순물인 경우에만 이 테스트를 수행하십시오.]
완충액: 약 1.3mL의 인산을 함유한 물 1L에 1.22g의 나트륨 1-데칸설폰산염. 20%(w/v) 수산화칼륨을 사용하여 pH 3.0으로 조정합니다.
이동상: 아세토니트릴 및 완충액(3:17)
시스템 적합성 솔루션: 이동상 내 USP Levetiracetam 관련 화합물 B RS 2 mg/mL
표준 용액: 이동상 내 USP 레베티라세탐 관련 화합물 B RS 0.002 mg/mL
샘플 용액: 이동상 내 레베티라세탐 2.0mg/mL
크로마토그래피 시스템
(크로마토그래피 621, 시스템 적합성 참조)
모드: LC
검출기: UV 200nm
컬럼: 4.6-mm × 25-cm; 포장 L1
유속: 1.0mL/분
주입 크기
시스템 적합성: 10 µL
분석: 50 µL
시스템 적합성
샘플: 시스템 적합성 솔루션
[참고-레베티라세탐 관련 화합물 B의 머무름 시간은 9분입니다.]
적합성 요구 사항
테일링 요인: NMT 3.0
[참고-레비티라세탐 관련 화합물 B 피크의 상당한 테일링이 관찰되는 경우(3.0 초과) 시스템을 안정화하기 위해 컬럼 온도를 27로 유지하는 것이 좋습니다.]
상대표준편차: NMT 2.0%
분석
시료: 표준용액 및 시료용액
레비티라세탐 섭취량 중 레비티라세탐 관련 화합물 B의 백분율을 계산합니다.
결과 = (rU/rS) × (CS/CU) × (Mr1/Mr2) × 100
rU = 검체 용액의 레베티라세탐 관련 화합물 B의 피크 반응
rS = 표준액의 레비티라세탐 관련 화합물 B의 피크 반응
CS = 표준 용액 내 USP 레베티라세탐 관련 화합물 B RS의 농도(mg/mL)
CU = 검체 용액 내 레베티라세탐 농도(mg/mL)
Mr1 = 레베티라세탐 관련 화합물 B 유리 염기의 분자량, 102.1
Mr2 = 레베티라세탐 관련 화합물 B의 분자량, 138.6
허용 기준: NMT 0.10%
[참고-레베티라세탐 유연물질B의 측정량은 유기불순물시험 제2법의 총불순물에 포함된다.]
• 절차 2
완충액, 용액 A, 용액 B, 이동상, 시스템 적합성 용액 및 크로마토그래피 시스템: 분석의 지시에 따라 진행합니다.
표준 용액: 용액 A에 포함된 USP 레베티라세탐 RS 0.005mg/mL
샘플 용액: 용액 A에 포함된 레베티라세탐 5mg/mL
분석
시료: 표준용액 및 시료용액
레베티라세탐을 섭취한 부분에서 각 불순물의 백분율을 계산합니다.
결과 = (rU/rS) × (CS/CU) × (1/F) × 100
rU = 샘플 용액의 각 불순물의 피크 반응
rS = 표준 용액의 레비티라세탐 피크 반응
CS = 표준 용액 내 USP 레베티라세탐 RS의 농도(mg/mL)
CU = 검체 용액 내 레베티라세탐 농도(mg/mL)
F = 상대 반응 인자(불순도 표 1 참조)
[참고-상대 유지 시간이 0.19 이하인 피크는 무시하십시오.]
합격기준
개별 불순물: 불순물 표 1을 참조하십시오.
총 불순물: NMT 0.4%
불순물 표 1
이름 상대 머무름 시간 상대 반응 인자 허용 기준, NMT(%)
피리딘-2-ol a 0.37 1.0 0.025
레베티라세탐산b 0.62 1.2 0.3
레베티라세탐 1.00 - -
레베티라세탐 관련 화합물 Ac 1.25 0.35 0.05
불특정 불순물 - 1.0 0.05
a 총 불순물 기준에는 포함되지 않습니다.
b (S)-2-(2-옥소피롤리딘-1-일)부탄산. 총 불순물 기준에 포함됩니다.
c (S)-N-(1-아미노-1-옥소부탄-2-일)-4-클로로부탄아미드. 레베티라세탐 관련 화합물 B가 알려진 공정 불순물인 경우에만 총 불순물 기준에 포함됩니다.
특정 테스트
• 수분 측정, 방법 Ia<921>: NMT 0.5%
• 레베티라세탐 R-에난티오머의 한계
이동상: n-헥산 및 탈수 알코올(4:1)
시스템 적합성 솔루션: 이동상 내 USP Levetiracetam Racemic Mixture RS 0.1mg/mL
표준 용액: 이동상 내 USP Levetiracetam RS 0.05mg/mL
샘플 용액: 이동상 내 레베티라세탐 10mg/mL
크로마토그래피 시스템
(크로마토그래피<621>, 시스템 적합성 참조)
모드: LC
검출기: UV 215nm
컬럼: 4.6-mm × 25-cm; 10-μm 패킹 L51
유속: 1.0mL/분
주입 크기: 20 µL
시스템 적합성
샘플: 시스템 적합성 솔루션
[참고-레비티라세탐 R-거울상 이성질체와 레베티라세탐 S-거울상 이성질체의 상대 체류 시간은 각각 0.55와 1.0입니다.]
적합성 요구 사항
해상도: R- 및 - 거울상 이성질체
[참고-분해능 손실(4.0 미만)이 관찰되는 경우 시스템 안정화를 위해 컬럼 온도를 25도로 유지하는 것이 좋습니다.]
분석
시료: 표준용액 및 시료용액
레비티라세탐 섭취량 중 레비티라세탐 R-거울상 이성질체의 백분율을 계산하십시오.
결과 = (rU/rS) × (CS/CU) × 100
rU = 시료 용액의 레베티라세탐 R-거울상 이성질체의 피크 반응
rS = 표준 용액의 레비티라세탐 피크 반응
CS = 표준 용액 내 USP 레베티라세탐 RS의 농도(mg/mL)
CU = 검체 용액 내 레베티라세탐 농도(mg/mL)
허용 기준: NMT 0.8%
추가 요구 사항
• 포장 및 보관: 잘 밀봉된 용기에 담아 실온에 보관하세요.
• USP 참조 표준<11>
USP 레베티라세탐 RS
USP 레베티라세탐 라세믹 혼합물 RS
레베티라세탐 S-에난티오머-(2S)-2-(2-옥소피롤리딘-1-일)부탄아미드와 레베티라세탐 R-에난티오머(2R)-2-(2-옥소피롤리딘-1-일)부탄아미드의 1:1 혼합물.
USP 레베티라세탐 관련 화합물 A RS
(S)-N-(1-아미노-1-옥소부탄-2-일)-4-클로로부탄아미드.
C8H14ClNO3 207.65
USP 레베티라세탐 관련 화합물 B RS
(S)-2-아미노부탄아미드 염산염.
C4H10N2O·HCl 138.6

필라세탐의 유도체인 레베티라세탐(CAS: 102767-28-2)은 1999년 미국 FDA의 승인을 받은 새로운 3세대 항간질제입니다. 초기에는 성인 부분 발작의 보조 치료로 사용되었습니다. 2005년에 레베티라세탐은 4세 이상 어린이의 부분 발작 보조 치료용 경구 정제 및 용액으로 승인되었습니다. 주로 성인과 4세 이상 소아의 부분발작에 대한 부가치료에 사용되며, 성인의 부분발작과 전신발작에만 사용할 수도 있다. 또한 청소년의 근간대성 간질, 난치성 간질, 어린이의 부재 간질 및 지속성 간질에 대한 특정 치료 효과가 있습니다.